
[베이비타임즈=최인환 기자] 식품의약품안전처(처장 김강립)는 코로나19 유행과 관련해 사회적 관심이 높아지고 있는 ‘코로나19 자가검사키트(이하 자가검사키트)’와 관련해 허가・조건부 허가 절차와 현황, 올바른 사용방법 등의 정보를 27일 알렸다.
먼저 자가검사키트는 '체외진단의료기기법'과 '민원 처리에 관한 법률' 등에서 정한 요건과 심사기준에 따라 허가・심사가 진행된다.
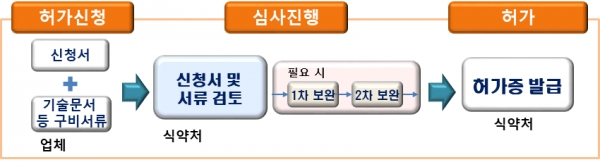
식약처는 제품의 허가(변경 허가 포함)신청이 접수되면 체외진단의료기기법에 따라 제출자료를 검토한다. 제출자료에 보완이 필요한 경우 민원 처리에 관한 법률에 따라 최대 2회 자료를 보완 및 제출하도록 요청하며, 최종 제출 자료가 적합하면 허가하고 그렇지 않으면 신청에 대해 반려 처분한다.
현재 국내에는 개인이 비강에서 검체를 채취하는 항원방식제품인 자가검사키트 3개가 허가를 받고 유통되고 있다. 해당 제품은 PCR 검사를 보조해 코로나19 바이러스의 존재 여부를 확인하는 제품이다.
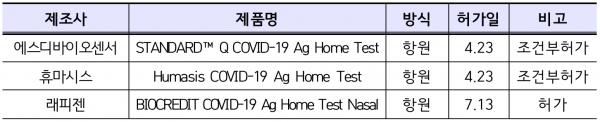
에스디바이오센서와 휴마시스 2개 제품은 조건부 허가 이행기한(7월 23일) 내에 최초 허가 시 부여된 조건을 삭제하기 위한 변경허가(법정 처리기한 60일)를 식약처에 신청했다. 현재 해당 2개 제품은 해외 임상적 성능시험 결과 성능이 입증돼 허가됐으며, 지금까지 품질의 문제는 발견되지 않아 유통과 사용은 가능하다. 하지만 식약처에서는 조건부 허가 요건을 이행하지 못하는 경우 필요한 행정조치를 검토할 예정이라고 밝혔다.
식약처 관계자는 "국내 임상적 성능시험기준 등을 충족한 제품만 국민들이 안심하고 사용할 수 있도록 제출된 자료를 신속하고 면밀하게 검토하겠다"며 "필요한 경우 보완 절차를 거쳐 허가조건 삭제 등 변경 허가 절차를 진행하겠다"고 밝혔다.
아울러 "자가검사키트는 코로나19 감염 진단이 아닌 보조 수단으로만 사용하고, 사용방법 및 주의사항 등을 준수해 사용해달라”고 당부했다.


